nội dung
Cục Quản lý dược (Bộ Y tế) vừa cho biết, cập nhật đến tháng 11.2025, có 46 công ty dược, cơ sở sản xuất thuốc nước ngoài có thuốc vi phạm chất lượng phải lấy mẫu kiểm tra chất lượng 100% lô thuốc nhập khẩu (tiền kiểm).
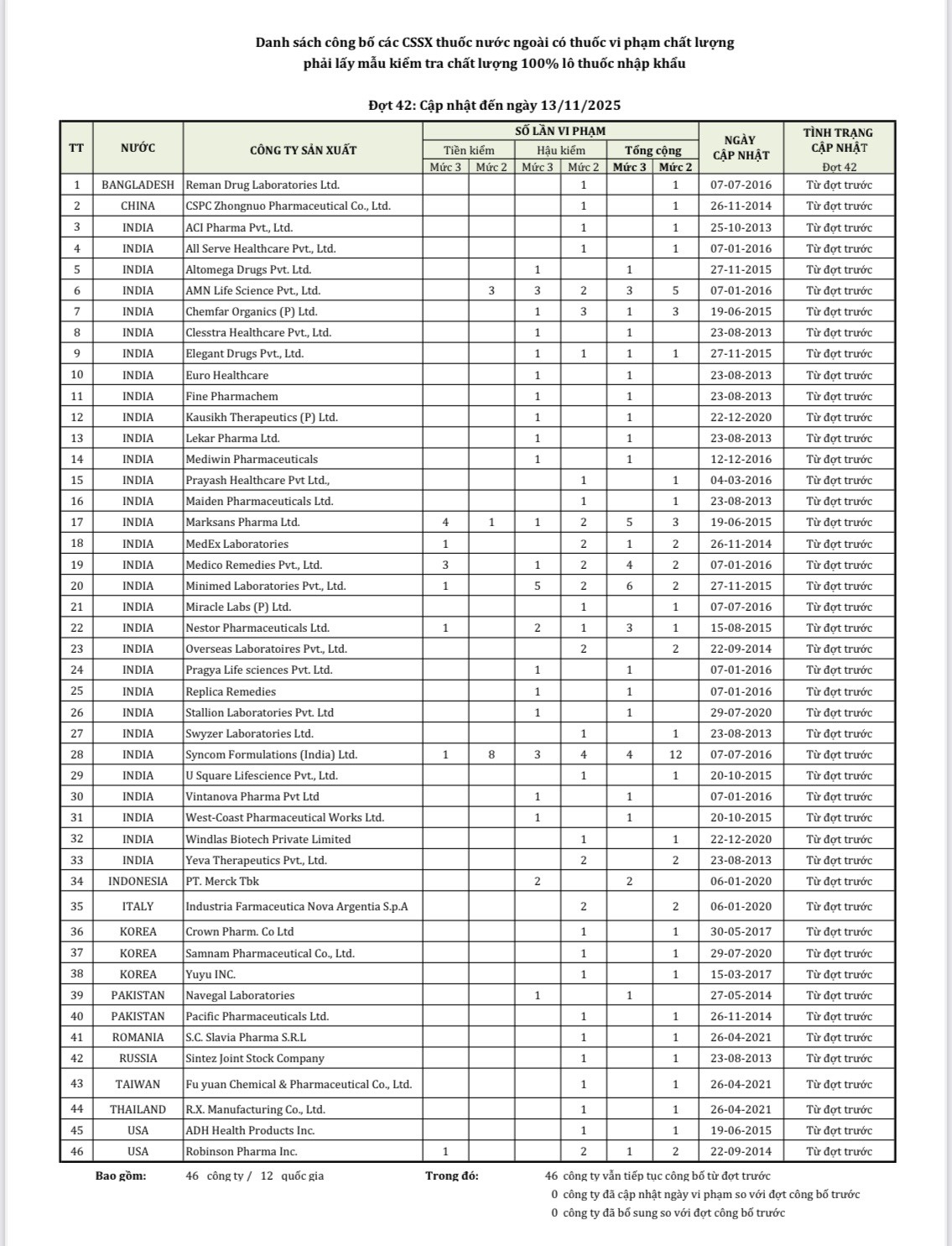
46 công ty dược của 12 quốc gia có thuốc vi phạm chất lượng phải tiền kiểm
ẢNH: DAV.GOV.VN
Theo danh sách công bố, có 31/46 là công ty dược của Ấn Độ; 3/46 của Hàn Quốc. Ngoài ra, còn có công ty của Pakistan, Thái Lan, Mỹ, Nga, Ý, Bangladesh, Trung Quốc, Romania…
Cục Quản lý dược đề nghị các sở y tế, y tế các ngành chỉ đạo các đơn vị quản lý dược, kiểm tra, kiểm nghiệm thuốc trực thuộc kiểm tra, giám sát việc chấp hành các quy định về kiểm tra chất lượng thuốc nhập khẩu và xử lý các tổ chức, cá nhân vi phạm theo quy định hiện hành.
Danh sách các công ty này được đăng tải trên trang thông tin điện tử của Cục Quản lý dược.
Ngoài ra, trong danh sách các thuốc, các cơ sở sản xuất vi phạm chất lượng thuốc, Cục Quản lý dược thông báo thu hồi thuốc Pyfaclor Kid (VD-26427-17), Cefaclor 125mg là cốm pha hỗn dịch uống (hộp 12 gói x 2g, hộp 14 gói x 2g, hộp 24 gói x 2g, số lô 410923, ngày sản xuất 13.9.2023, hạn dùng 130926 của Công ty cổ phần dược phẩm Pymepharco.
Cục Quản lý dược cũng thông báo 98 công ty, cơ sở sản xuất thuốc nước ngoài của 16 quốc gia đã rút khỏi danh sách vi phạm về chất lượng thuốc.
Theo quy định hiện hành, thời hạn kiểm nghiệm tính từ thời điểm lô thuốc đầu tiên được nhập khẩu sau thời điểm Bộ Y tế (Cục Quản lý dược) công bố danh sách cơ sở sản xuất có thuốc vi phạm chất lượng như sau:
Giới thiệu về sản phẩm này
Độ chính xác đo: + / - 0,5% FS
Dung sai bù đầu lạnh: + /- 2 độ C (có thể được sửa đổi
bằng phần mếm trong 0 ~ 50 độ C)
Độ phân giải: 14 bit
Chu ky lấy mẫu: 0,5 giây
Quyền lực: AC 100-240V 50 / 60HZ
Giá trị quá trình (PV), Giá trị cài đặt (SV)
<iểm soát PIN (bao gồm ON / OFF, PID loại bước và PID liêr
tỤc)
Điều khiển tự điều chỉnh
Đầu ra rơ le: công suất tiếp xúc 250V AC 3A (tải điện
3ộ điều khiển nhiệt độ PID REX-C100, với cặp nhiệt
6 tháng đối với cơ sở sản xuất có không quá 2 lô thuốc vi phạm chất lượng ở mức độ 3; 12 tháng đối với cơ sở sản xuất có 1 lô thuốc vi phạm chất lượng ở mức độ 2 hoặc có từ 3 lô thuốc vi phạm chất lượng ở mức độ 3 trở lên; 24 tháng đối với cơ sở sản xuất có 1 lô thuốc vi phạm chất lượng ở mức độ 1 hoặc có từ 2 lô thuốc vi phạm chất lượng ở mức độ 2 trở lên…
Bài viết gợi ý
- 5 loại rau ăn nhiều "phá gan", ngon bổ mấy cũng hạn chế
Rau vốn là thực phẩm tốt cho sức khỏe, giàu dinh dưỡng. Tuy nhiên, một số loại rau củ nếu chế biến hoặc bảo quản không đúng cách có thể tăng gánh nặng cho gan, thậm chí gây t...
- Nhìn từ iPhone 17: Đã đến lúc hai "đầu tàu" Android nên nói lời chia tay với dung lượng 128GB
- CAHN và Bắc Kinh Quốc An cùng nhận án phạt ở giải châu Á
- Thi lại đại học, chàng trai quê Hưng Yên thành thủ khoa đặc công nước
- Cách cài đặt thời gian tắt màn hình máy tính Windows đơn giản nhất
- 3 nét tướng “vàng” nơi công sở: Nhìn là biết ai dễ thăng chức, sự nghiệp lên hương
- 4 con giáp làm gì cũng thuận, quý nhân đến tận cửa trong tuần mới
- Sau vụ ngộ độc ở TP.HCM: Nhiều người e dè ăn bánh mì, sợ nguyên liệu 'trôi nổi'
